Les dispositifs de surveillance des résistances aux antibiotiques et de la consommation d'antibiotiques permettent de suivre l’évolution de ces enjeux de santé publique majeurs.
Reprise de la consommation d’antibiotiques à l’hôpital en 2022
En 2022, la surveillance des consommations d’antibiotiques par la mission Spares, animée par le CPias Grand-Est et le CPias Nouvelle-Aquitaine, et pilotée par Santé publique France, rapporte une consommation globale des ES participants de 296 doses définies journalières (DDJ) pour 1 000 journées d’hospitalisation (JH), ce qui représente une augmentation marquée. Ce résultat porte sur 1 573 établissements de santé (ES)volontaires, représentant environ 80 % des journées d’hospitalisation (JH) en France.
doses définies journalières / 1 000 journées d'hospitalisation
Une consommation d’antibiotiques variable selon les secteurs d’activité
La quantité et la nature des antibiotiques utilisés variaient selon le secteur d’activité clinique.
En psychiatrie, soins de longue durée et gynécologie-obstétrique, les antibiotiques majoritairement utilisés étaient l’amoxicilline associée ou non à l’acide clavulanique alors qu’en réanimation, hématologie et maladies infectieuses, une grande variété d’antibiotiques était utilisée, en lien avec les pathologies infectieuses prises en charge dans ces différents secteurs d’activité. Les carbapénèmes, les glycopeptides et la daptomycine étaient surtout utilisés dans les secteurs de réanimation, de médecine, en chirurgie et en pédiatrie.
En pédiatrie, les doses utilisées pour traiter un enfant étant plus faibles, l’exposition des enfants hospitalisés est sous-estimée car, par convention, la « dose standard » utilisée pour mesurer les consommations d’antibiotiques est définie pour un adulte de 70 kg (ainsi, une « dose standard » correspond à plusieurs doses enfants utilisées).
Une consommation variable en fonction des antibiotiques
Sur la période 2012-2022, la consommation de certains antibiotiques ou familles d’antibiotiques a diminué : fluoroquinolones, glycopeptides et association amoxicilline/acide clavulanique notamment, alors que la consommation d’autres antibiotiques a progressé : association pipéracilline-tazobactam, céphalosporines de 3e génération, carbapénèmes, linézolide et daptomycine.
Globalement, la part d’antibiotiques à large spectre et de certains antibiotiques actifs sur les staphylocoques résistants à la méticilline dans la consommation globale a progressé durant la période.
A lire aussi
Prévention de la résistance aux antibiotiques : une démarche "une seule santé" - Novembre 2023
Prescriptions d’antibiotiques en médecine de ville : reprise confirmée en 2022
Surveillance de la consommation des antibiotiques et des résistances bactériennes en établissement de santé. Mission Spares. Résultats ...
Consommation d’antibiotiques en ville : des évolutions encourageantes
Quelle consommation en ville en France en 2022 ?
- La consommation globale des antibiotiques en secteur de ville est estimée en 2022 à 21,6 DDJ/1000 hab/j ou 821,5 prescriptions pour 1000 habitants et par an.
- La consommation varie significativement selon l'âge et le sexe du patient. Elle est globalement plus élevée chez les femmes que chez les hommes. Elle est plus élevée chez les enfants de 0 à 4 ans et chez les adultes de 65 ans et plus ; elle est plus faible chez les 5-14 ans1.
- Les antibiotiques les plus consommés en 2022 sont les bêta-lactamines parmi lesquels l’amoxicilline, prescrite en première intention en accord avec les fiches pour le choix et les durées d'antibiothérapie préconisées dans les infections bactériennes courantes publiées par la Haute Autorité de santé et les recommandations émises par plusieurs sociétés savantes.
Quelles évolutions en ville entre 2012 et 2022 ?
- La consommation d’antibiotiques en secteur de ville a connu une baisse régulière et modérée entre 2012 et 2019. En 2020, elle a fortement diminué, principalement en raison de la pandémie de COVID-19 qui a entraîné une baisse des recours aux soins courants en ville, et donc moins de prescriptions, en particulier durant le premier confinement. La pandémie a également modifié les comportements individuels et contribué à un renforcement des mesures d’hygiène prévenant les infections bactériennes.
- En 2021, la consommation d’antibiotiques est repartie à la hausse : + 4,9 % en DDJ et + 6 % en prescriptions mais elle demeure plus basse qu’en 2019. Cette augmentation s'explique notamment par le fait que l’année 2021 a été marquée par des périodes de confinement beaucoup plus courtes qu’en 2020 ainsi que par le retour des infections saisonnières habituelles, dont la prévalence avait été beaucoup plus faible en 20202.
- Les pratiques médicales ont évolué : en cohérence avec les recommandations de bonne pratique, on observe sur la période 2011-2021 une évolution des types d’antibiotiques prescrits, avec une augmentation de la consommation des bêta-lactamines (pénicillines à large spectre dont l’amoxicilline) et une diminution de la consommation de céphalosporines (antibiotiques plus fortement générateurs de résistance).
- En 2022, la consommation d’antibiotiques a de nouveau progressé : + 14% en DDJ et + 16,6% en prescriptions. Elle demeure cependant un peu plus faible qu’en 2019.
- La forte reprise de la consommation en 2022 peut s'expliquer principalement par une prescription plus fréquente d'antibiotiques, lors d'une consultation ou d'une visite, notamment pour traiter des pathologies – souvent hivernales – courantes. Ainsi en ce qui concerne les syndromes grippaux, la saison 2022-2023 s'est caractérisée par une épidémie exceptionnellement longue et précoce et a ainsi contribué à la forte progression de la consommation observée en fin d'année.
- De même, les gastro-entérites aigües – qui peuvent donner lieu à des traitements antibiotiques, même si elles sont souvent d'origine virale - ont retrouvé des niveaux comparables à ceux d'avant la pandémie.
1 Il est rappelé que si les prescriptions peuvent être comparées entre elles, quelle que soit la tranche d'âge, cela n'est pas possible pour l'indicateur DDJ. En effet, il n'existe pas de DDJ pédiatrique et la conversion des consommations des enfants sur la base des DDJ "adultes" conduit à sous-estimer leur consommation.
2 Source : Santé Publique France "Bilan préliminaire de l’épidémie de grippe 2021-2022", publié le 01/06/2022 et bulletin épidémiologique gastro-entérite aiguë, semaine 52. Saison 2021-2022.
Des résultats hétérogènes selon les régions
Des disparités de consommation sont constatées au niveau territorial (données accessibles via Géodes). Leur analyse est toutefois complexe. En effet, de nombreux éléments doivent être pris en compte pour interpréter correctement les écarts observés. L’état de santé de la population, l’espérance de vie, l’offre de soins, l’activité médicale mais également la pyramide des âges varient d’une région à l’autre. Ils induisent des recours différenciés au système de soins et donc des niveaux de consommation d’antibiotiques différents.
Entre 2010 et 2019, la consommation d’antibiotiques, exprimée en DDJ, est demeurée stable ou en légère diminution dans la plupart des régions ; parallèlement, le nombre de prescriptions a diminué dans presque toutes les régions. En 2020, quel que soit l’indicateur retenu, la consommation a fortement diminué dans toutes les régions. Les évolutions intra régionales ne diffèrent pas notablement de la tendance observée au niveau national. En 2021 et en 2022, la reprise des consommations n'est pas constatée dans toutes les régions.
Quelle que soit l’année considérée, la consommation d’antibiotiques est toujours plus faible dans les régions d’Outre-Mer. En Métropole, les niveaux de consommation régionale les plus élevés sont observés dans les Hauts-de-France, en Provence-Alpes-Côte d'Azur et en Corse.
Ces différences justifient que les actions nationales en faveur du bon usage antibiotique soient déclinées et adaptées pour chaque territoire.
En savoir plus
Prescriptions d’antibiotiques en médecine de ville : reprise confirmée en 2022
La reprise de la consommation d’antibiotiques en secteur de ville se confirme en 2022
Consommation d’antibiotiques en Ehpad : premiers indicateurs nationaux pour les Ehpad sans PUI
Quelle consommation d'antibiotiques en 2022 ?
- Les données concernant les résidents en Ehpad sans pharmacie à usage intérieur (PUI) qui font l’objet d’un remboursement individuel par l’Assurance maladie sont extraites depuis 2021. Ces données portent sur les consommations d'antibiotiques et sur les durées d'hébergement. Elles ont permis de produire des indicateurs spécifiques aux résidents en Ehpad sans PUI (84% des établissements en 2015) pour la période 2015-2022.
- Entre 2015 et 2022, la consommation d'antibiotiques dans les EHPAD sans PUI a été orientée à la baisse et, comme dans le secteur de ville, une très forte diminution a été observée en 2020. Mais contrairement au secteur de ville (pris dans son intégralité), la consommation a continué de diminuer en 2021 (-10,3 en DDJ et -9,6% en prescriptions). Ces évolutions divergentes s'expliquent notamment par le fait que les protocoles mis en place dans les Ehpad pour assurer la protection des résidents n'ont été assouplis qu'en mai puis en août 2021, et l'ensemble des gestes barrières a continué à être respecté, notamment le port du masque en intérieur.
- En 2022, par contre, la consommation a augmenté. Elle s'est établie à 40,5/DDJ/1000 Jheb (+11,4% par rapport à 2021) et 4,07 presc/1000 Jheb (+10,5% par rapport à 2021). Le retour progressif à des protocoles proches de ceux en vigueur avant la pandémie permet en partie d'expliquer les augmentations constatées.
- La consommation a diminué dans presque toutes les classes d'antibiotiques, sauf la famille des sulfonamides et trimethoprime, et la famille des tétracyclines.
- La consommation et les prescriptions de nitrofurantoïne ont fortement diminué et se sont reportées versla fosfomycine.
- L'amoxicilline ainsi que l’association de l'amoxicilline avec un inhibiteur d'enzyme sont les antibiotiques les plus prescrits et le plus consommés pendant toute la période.
Consommation d’antibiotiques en Ehpad avec PUI
Les données présentées sont issues d’une enquête nationale réalisée par la Mission SPARES sur la consommation d’antibiotiques des résidents en EHPAD qui disposent d’une pharmacie à usage intérieure (PUI).
Quelle consommation d'antibiotiques en 2022 ?
- La consommation globale dans les EHPAD participants est estimée à 30,7 Doses Définies Journalières (DDJ) pour 1000 journées d’hébergement (JHeb).
Quelles évolutions entre 2018 et 2022 ?
- La consommation globale d’antibiotiques a diminué de 10% par rapport à 2018 (34 DDJ/1 000 JHeb en 2022, 38,2 en 2018) dans une cohorte de 220 Ehpad avec PUI ayant transmis des données chaque année.
- En EHPAD, l’amoxicilline-acide clavulanique et l’amoxicilline sont les antibiotiques les plus consommés et représentaient respectivement 35% et 24% des antibiotiques en 2022. A noter que l’association amoxicilline-acide clavulanique est, selon la classification de la Spilf, un antibiotique « à indications restreintes, ayant un impact plus important sur la résistance bactérienne ». En raison du poids de cet antibiotique dans la consommation totale, la part représentée par ces antibiotiques « à indications restreintes » est majoritaire en Ehpad et a même progressé entre 2018 et 2022 de 53% à 56%.
- À l’inverse, la consommation d’azithromycine reste plus élevée en 2021 qu'en 2018 et 2019. La prise en charge de patients Covid-19, chez lesquels une pneumonie bactérienne a parfois pu être suspectée, explique la progression du recours à la ceftriaxone et à l’azithromycine, en particulier en début d’épidémie. Elle est cepedant plus faible en 2021 qu'en 2020, en lien avec les recommandations émises pour la prise en charge des patients positifs à la COVID-19.
Une vigilance à maintenir sur les infections à entérobactéries résistantes aux antibiotiques
En établissements de santé
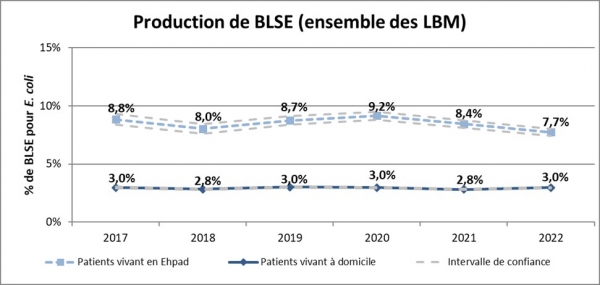
L’incidence des infections à entérobactéries productrices de béta-lactamase à spectre étendu isolées de tous prélèvements à visée diagnostique réalisés en établissements de santé a augmenté de 27 à 71 cas pour 100 000 journées d’hospitalisation entre 2008 et 2016. A partir de 2016, une baisse s’est amorcée avec 67 cas en 2017, 63 cas en 2018 et 53 cas en 2019 (avec une méthode un peu différente) pour 100 000 journées d’hospitalisation. Cependant, en 2020, l’incidence des EBLSE a augmenté de nouveau avec 58 cas pour 100 000 JH dans le contexte COVID-19. En 2022, l’incidence est revenue à un niveau similaire à 2019 avec 54 cas pour 100 000 JH.
En établissement de santé, la proportion de résistance aux fluoroquinolones chez les souches d’E. coli isolées d’une infection invasive concerne 14,7 % des souches en 2022. Elle est globalement à la baisse depuis 2012.
Les efforts de maîtrise de la transmission croisée et de meilleur usage des antibiotiques en établissement de santé sont donc à poursuivre sans relâche pour conforter cette évolution positive.
Les DI de SARM observées en 2022 étaient plus faibles qu’en 2021. Celle des EBLSE est supérieure à ce qu’elle était en 2022 (
Sur la période 2018-2022, la DI des SARM amorce une nouvelle diminution. La tendance des EBLSE est globalement stable entre 52 et à 54 cas pour 100 000 JH, avec une augmentation ponctuelle à 58 cas en 2020.
Prévention de la résistance aux antibiotiques : une démarche "une seule santé" - Novembre 2023
Surveillance de la consommation des antibiotiques et des résistances bactériennes en établissement de santé. Mission Spares. Résultats ...
Des progrès en ville comme en Ehpad concernant la résistance aux céphalosporines de 3e génération, mais vigilance concernant la résistance aux fluoroquinolones
Baisse de la résistance de la bactérie E. coli aux céphalosporines de 3e génération (C3G) en ville comme en Ehpad
Escherichia coli est la bactérie la plus fréquemment isolée en laboratoire de ville (9 bactéries sur 10) : elle est en particulier responsable d’infections urinaires.
- En ville, la proportion de résistance aux céphalosporines de 3e génération chez les souches d’E. coli isolées d’un prélèvement urinaire concerne 3,3 % des souches isolées en 2022. Elle a augmenté de 2,3 % en 2012 à 4,2 % en 2015. Elle a diminué de 4,2% en 2015 à 3,2% en 2018. Depuis, elle est stable entre 3,2% et 3,4%.. Parallèlement, la proportion de souches productrice de béta-lactamase à spectre étendu est plutôt stable sur la période 2017-2022 entre 3,0% et 2,8% (3,0% en 2022).
- En Ehpad, la proportion de résistance aux céphalosporines de 3e génération chez les souches d’E. coli isolées d’un prélèvement urinaire est, plus élevée que pour les patients de ville. Elle concerne 8,5 % des souches en 2022. Après avoir fortement augmenté de 8,0 % en 2012 à 11,1 % en 2015, cette proportion était en diminution par rapport à 2017 (9,9 %).
Evolution entre 2017 et 2022 de souches E. coli productrices de BLSE isolées d'un prélèvement urinaire chez les patients vivant à domicile et en Ehpad, France, Mission Primo
Hausse en ville et baisse en Ehpad de la résistance aux fluoroquinolones
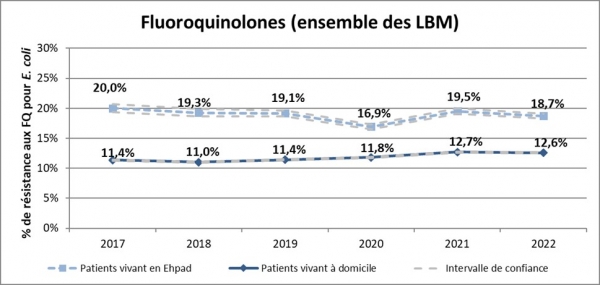
- En ville, la proportion de résistance aux fluoroquinolones chez les souches d’E. coli isolées d’un prélèvement urinaire concerne 12,6 % des souches isolées en 2022. Elle a marqué une tendance à la baisse de 12,5 % en 2013 à 11,0 % en 2018, mais elle s’oriente à la hausse depuis 2018, avec une augmentation plus marquée en 2021 (+7,6 % par rapport à 2020).
- En Ehpad, la proportion de résistance aux fluoroquinolones chez les souches d’E. coli isolées d’un prélèvement urinaire concerne 18,7 % des souches en 2022. Après avoir marqué une forte diminution de 27,8 % en 2013 à 16,9 % en 2020, l’augmentation observée en 2021 semble s’affichée comme une augmentation ponctuelle qui ne se poursuit pas en 2022.
Ces résultats montrent que la lutte contre l’antibiorésistance reste un enjeu majeur de santé publique.
Evolution entre 2017 et 2022 de la proportion de résistance aux fluoroquinolones chez E. coli isolées d'un prélèvement urinaire chez les patients vivant à domicile et en Ehpad, France, Mission Primo
A lire aussi
Prévention de la résistance aux antibiotiques : une démarche "une seule santé" - Novembre 2023
Surveillance de la résistance bactérienne aux antibiotiques en soins de ville et en établissements pour personnes âgées dépendantes. Mi...
La situation européenne
Au niveau européen, des données sont disponibles à travers le réseau EARS-Net pour deux espèces d’entérobactéries : Escherichia coli, (entérobactérie présente dans le tube digestif et fréquemment responsable d’infection, au premier plan desquelles l’infection urinaire) et chez Klebsiella pneumoniae.
Dans ces deux espèces bactériennes, la proportion de résistance aux céphalosporines de 3ème génération a fortement augmenté depuis 2006.
En 2021, la proportion moyenne (pondérée par la population des pays participants au réseau) de résistance aux C3G chez Escherichia coli est de 14,3%. Avec 8,4%, la France se situe sous la moyenne européenne. Sur la période 2018-2022, la proportion moyenne européenne de résistance aux céphalosporines de 3e génération chez E. coli a diminué de 15,7% à 14,3%. En France, la tendance est également à la diminution puisque en 2017, la proportion était de 10,2%.
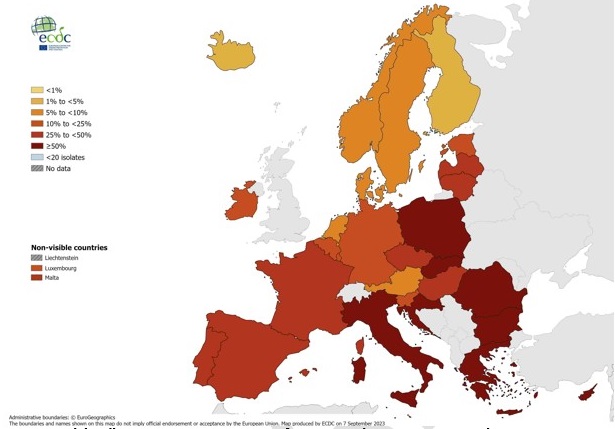
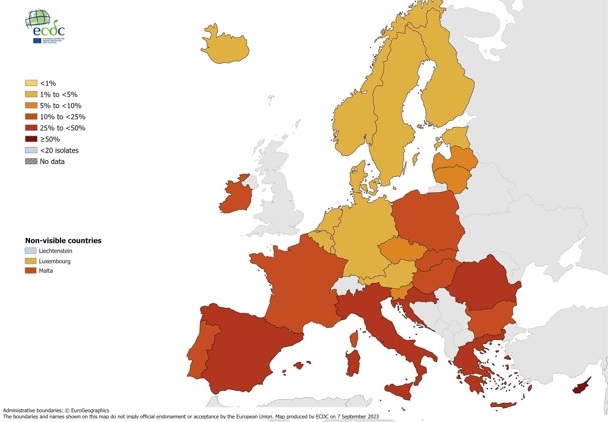
Concernant Klebsiella pneumoniae, la proportion moyenne (pondérée par la population des pays participants au réseau) de résistance aux C3G est de 32,7%. Sur la période 2018-2022, la proportion moyenne européenne de résistance aux céphalosporines de 3e génération chez K. pneumoniae est à la baisse (34,4% en 2018). En France, la tendance est aussi à la baisse, avec 30,8% en 2018 et 25,0% en 2022.
Proportion de résistance aux céphalosporines de 3e génération chez les souches de Klebsiella pneumoniae isolées d’infections invasives, Europe, 2022.
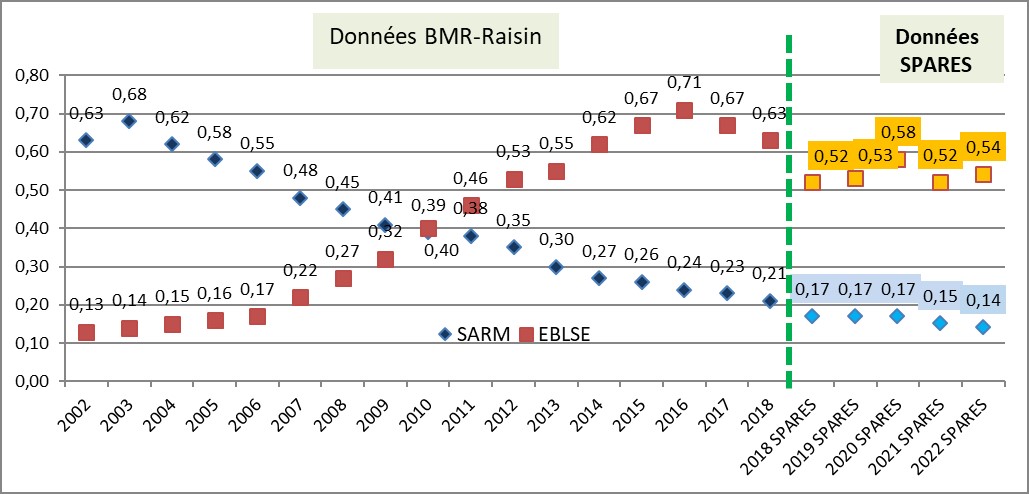
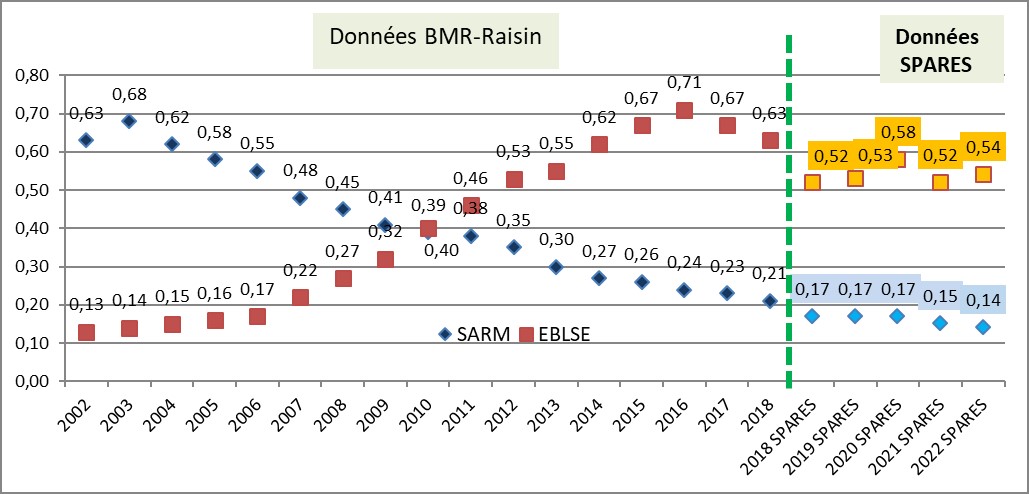
Une diminution constante de Staphylococcus aureus résistants à la méticilline (SARM)
La situation est plus favorable pour le staphylocoque doré résistant à la méticilline (SARM) puisqu’on constate une diminution constante des infections à SARM entre 2003 et 2022.
En 2022, la mission Spares rapporte une incidence des SARM de 0,14 souche pour 1000 JH, avec une valeur presque 4 fois plus élevée en réanimation et l'incidence des EBLSE était de 0,54 souche pour 1000 JH, avec une valeur 6 fois plus élevée en réanimation.
Evolution entre 2002 et 2022 de l’incidence (nombre de souches pour 1000 JH) des SARM et des EBLSE (nombre d’établissements participants variable chaque année, changement de méthode de surveillance en 2018).
En savoir plus
Prévention de la résistance aux antibiotiques : une démarche "une seule santé" - Novembre 2023
Surveillance de la consommation des antibiotiques et des résistances bactériennes en établissement de santé. Mission Spares. Résultats ...
Au niveau européen, le réseau EARS-Net rapporte une proportion moyenne (pondérée par la population des pays participants au réseau) de résistance à la méticilline chez le staphylocoque doré égale à 15,2% en 2022. Avec 10,4%, la France se situe légèrement sous la moyenne européenne. Sur la période 2018-2022, la proportion moyenne européenne de résistance la méticilline chez le staphylocoque doré a diminué de 17,8% en 2018 à 15,2% en 2022.
Elle a également diminué en France.
Risque d’impasse thérapeutique : les bactéries hautement résistantes aux antibiotiques émergentes
Les bactéries hautement résistantes émergentes (BHRe) sont des bactéries présentes naturellement dans le corps humain, qui sont devenues résistantes à quasiment tous les traitements antibiotiques utilisés habituellement pour les traiter. Il devient alors très difficile, voire impossible de traiter le patient qui présente une infection à BHRe.
Deux types de bactéries sont définis comme BHRe : les entérobactéries productrices de carbapénèmases (EPC), et Enterococcus faecium résistant aux glycopeptides (ERG). Il existe en France des recommandations particulières de prise en charge des patients infectés ou porteurs d'une BHRe, dont l'actualisation a été publiée en janvier 2020.
Chaque année, Santé publique France réalise un bilan sur la situation des BHRe en France, à partir des données du signalement externe des infections associées aux soins.
Depuis 2012, le nombre de signalements rapportant une EPC ou un ERG est en augmentation constante. Cependant, dans le contexte de l’épidémie de COVID-19, l’année 2020 a été marquée par une diminution importante des signalements d’EPC (- 38%) et de ceux d’ERG (- 45%).
En 2022, les signalements (SIN) de BHRe ont augmenté à nouveau, notamment ceux d’EPC, pour dépasser le nombre de SIN de 2019. La diminution du nombre de SIN d’épisodes mettant en cause une ou plusieurs BHRe observée en 2020 et 2021 peut s’expliquer par plusieurs hypothèses : 1) une diminution des transmissions de BHRe en raison des mesures de contrôle renforcées mises en place pour la pandémie COVID-19 ; 2) une diminution des dépistages autour des cas ; ou 3) une sous-déclaration probable des signalements BHRe au profit des très nombreux signalements COVID-19.
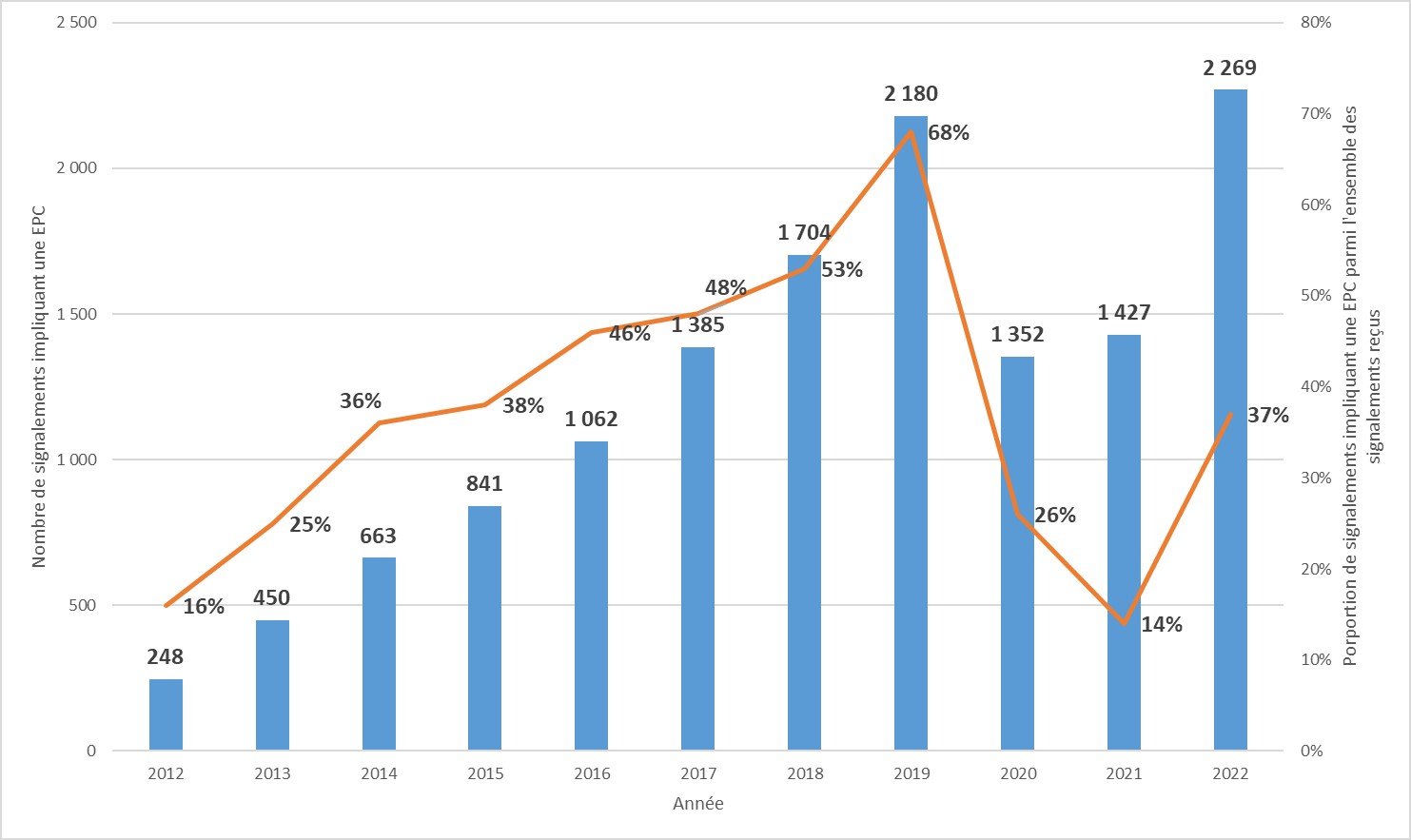
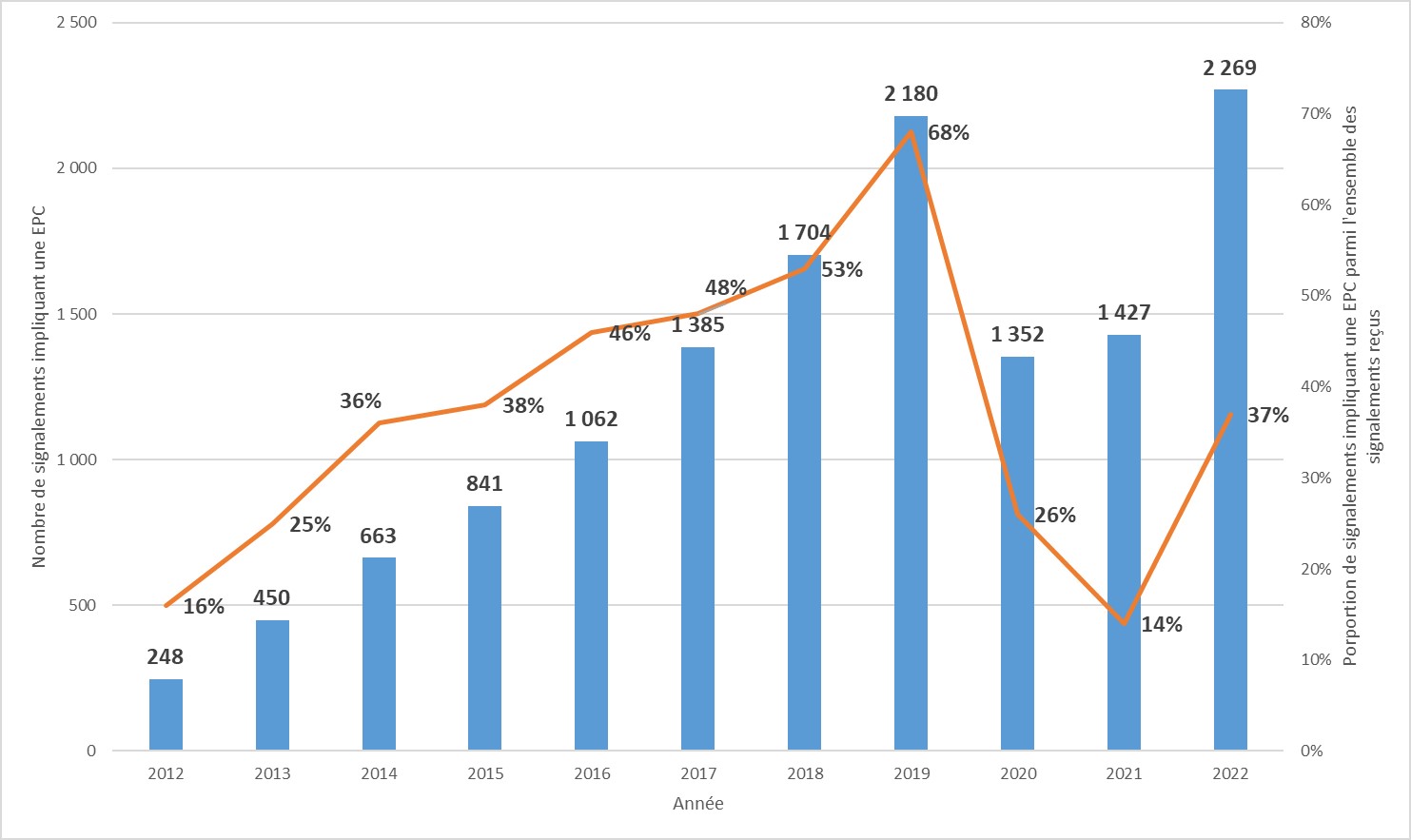
La mention d’un lien avec l’étranger était plus fréquente en 2022 qu’en 2021 et 2020.
La proportion des prélèvements cliniques à visée diagnostique augmente ce qui suggère une moindre identification et ou recherche de cas colonisés.
On observe une diminution de la mise en œuvre des précautions complémentaires contact à l’admission des cas ainsi que des mesures spécifiques lors de l’identification d’un cas, notamment pour les EPC.
Enfin, le suivi des indicateurs du PROPIAS montre que la proportion de cas secondaires parmi les cas d’EPC et d’ERG a augmenté.
Ces constats font craindre un risque de diffusion non identifiée d’EPC et d’ERG. La vigilance et les efforts pour maitriser la diffusion des BHRe dans les ES doivent être renforcés.
Ces données sont à mettre en parallèle de celles disponibles dans les réseaux de surveillance : les données françaises du réseau EARS-net montrent une proportion de résistance aux carbapénèmes chez les entérobactéries isolées d’hémoculture ou de LCR qui se maintient à moins de 1% depuis plusieurs années.
Les EPC et les ERG ne sont responsables que de peu d’infections graves en France. La dernière enquête de prévalence des infections associées aux soins en établissements de santé (ENP) rapportait également qu’en 2017 0,65 % (IC95% [0,26-1,60]) des entérobactéries testées étaient résistances aux carbapénèmes, soit une prévalence des patients infectés par des souches résistantes aux carbapénèmes égale à 0,01% (IC95% [<0,01-0,03]). Concernant les ERG, la proportion de résistance aux glycopeptides chez les souches isolées d’hémoculture est là encore inférieure à 1%. De même, l’ENP montre une proportion de résistance aux glycopeptides 5,07% (IC95% [2,16-11,43]) parmi les souches de E. faecium. Ceci correspond à une prévalence de patients infectés à E. faecium résistants aux glycopeptides inférieure à 0,01%. Une actualisation de ces prévalences à partir de l’ENP conduite en mai-juin 2022 sera prochainement disponible.
Cette situation est possible grâce à la promotion de la stratégie « search and isolate », mise en place dans les établissements de santé français, suite aux recommandations du Haut Conseil de la Santé Publique (HCSP) actualisées en 2020 (parues initialement en 2013), afin de prévenir la diffusion des BHRe. Mais, les dernières données du CNR de la résistance aux antibiotiques nous invitent à rester vigilants. Les efforts de maîtrise de la diffusion des EPC et des ERG dans les établissements de santé restent d’actualité et doivent même être renforcés, d’autant que d’une manière plus générale, la stratégie de dépistage semble s’infléchir en 2020, en contexte de pandémie Covid19, laissant craindre une diffusion à bas bruit des BHRe.
Données de résistance chez les autres pathogènes usuels
Le tableau ci-dessous reprend les données actualisées disponibles pour les principales espèces bactériennes pathogènes de l’homme faisant l’objet de dossiers thématiques spécifiques. Les phénomènes de résistances chez ces espèces revêtent un intérêt de santé publique au vu des échecs thérapeutiques dont ils peuvent être responsables.
Les données reprises ici sont principalement issues des réseaux de surveillance animés par les CNR en lien avec Santé publique France.
Les souches bactériennes résistantes aux antibiotiques sont des souches pour lesquelles il existe une forte probabilité d’échec thérapeutique quel que soit le type de traitement et la dose d’antibiotique utilisée. Les seuils de résistances aux différents antibiotiques pour chaque espèce bactérienne sont définis chaque année par le comité de l’antibiogramme de la société française de microbiologie (CA-SFM). Néanmoins, des seuils de résistance différents peuvent être retenus afin de disposer de données comparables aux données internationales (cf. Neisseria gonorrheae). Pour les antifongiques, les seuils d'interprétation utilisés par le CNR sont ceux définis par le CLSI (clinical and Laboratory standard institute) en attendant ceux du comité EUCAST.
Le fardeau des infections à bactéries résistantes aux antibiotiques en France et en Europe
Faire prendre conscience de l’impact en santé publique de la résistance aux antibiotiques est complexe : les systèmes de surveillance ciblent des couples bactéries/antibiotiques spécifiques, et sont même parfois restreints à des types de prélèvements. Difficile de faire comprendre à un public non professionnel ce que représente, par exemple, l’incidence des prélèvements diagnostics positifs à SARM (Staphylococcus aureus résistant à la méthicilline), l’un des couples bactéries/antibiotiques le plus fréquemment rencontré en milieu hospitalier. Il est donc nécessaire de disposer d’indicateurs complémentaires, permettant d’aborder le sujet d’une manière globale et plus facilement appréhendables par tout le monde. C’est l’objet de cette étude européenne, coordonnée par le European Center for disease prevention and control (ECDC), à laquelle Santé publique France a participé, qui avait pour objectif d’estimer un nombre de cas, un nombre de décès et un nombre de DALY (Disability adjusted life years) attribués aux infections à bactéries multirésistantes en Europe. L’indicateur DALY prend en compte le nombre total d’années perdues à cause d’un décès ou d’une incapacité, ici à la suite d’une infection à bactérie multirésistante. Il a donc l’intérêt de tenir compte de la durée de vie impactée par une maladie avant le décès. L’Organisation mondiale de la santé l’utilise dans d’autres études sur l’impact global des maladies. Il est donc possible de comparer le poids des maladies entre elles, ce qui peut aider à prioriser les actions de prévention.
Les résultats de cette étude ont été publiés en novembre 2022.
L’étude Burden
Avant l'étude européenne, une étude française avait déjà été réalisée par Santé publique France pour estimer le nombre de cas et le nombre de décès liés à des infections à bactéries multirésistantes survenus en France en 2012.
L’étude Burden BMR réalisée par Santé publique France en 2014-2015 avait pour objectif d’estimer le poids en santé publique (morbidité, mortalité) des infections à bactéries multirésistantes en France. 7 bactéries multirésistantes ont été retenues pour cette étude : Staphylococcus aureus résistant à la méticilline (SARM), entérocoques résistants à la vancomycine, Escherichia coli et Klebsiella pneumoniae résistant aux céphalosporines de 3e génération (C3G), K. pneumoniae, Acinetobacter spp. et Pseudomonas aeruginosa résistant aux carbapénèmes. L’incidence des infections invasives dues à ces BMR (données EARS-Net, 2012) a été redressée et extrapolée aux autres sites infectieux, et la mortalité attribuable à ces infections estimée en utilisant des ratios issus de la littérature.
Trois chiffres clés à retenir :
- 158 000 cas d’infections à BMR par an en France, dont 16 000 infections invasives (infections graves : méningites, bactériémies, septicémies) ;
- 12 500 décès associés à ces infections ;
- l’étude Burden BMR confirme que le poids des infections à BMR est très important ; les infections à SARM et entérobactéries résistantes aux C3G en représentent la plus grande part (deux tiers du total des infections recensées).

